Onderzoekers van de Michigan State onthullen de moleculaire werking van hoe bepaalde vormen van uitgezaaide borstkanker zich naar andere delen van het lichaam verspreiden. Door dit te doen, creëren ze nieuwe mogelijkheden om zogenaamde negatieve triple borstkanker op te sporen en in te dammen.
MSU universitair hoofddocent Sophia Lunt
“We hebben ons gericht op triple-negatieve borstkanker, of TNBC, omdat het proportioneel vaker voorkomt bij jongere patiënten en een slechtere klinische uitkomst heeft”, zei Dr. Sophia Lunteen professor bij College voor Natuurwetenschappen bij MSU.
“De meeste TNBC-gerelateerde sterfgevallen worden veroorzaakt door metastase, de verspreiding van kankercellen van de primaire tumor naar andere plaatsen in het lichaam,” zei Lunt. “Uitgezaaide borstkanker is ongeneeslijk en de beschikbare behandelingen zijn alleen bedoeld om de progressie van de ziekte te vertragen.”
Sinds hij in 2015 bij MSU kwam werken, heeft Lunt’s onderzoek zich gericht op het begrijpen van de rol van het metabolisme – welke voedingsstoffen en verbindingen kankercellen gebruiken en hoe – bij metastase. Hij en zijn team rapporteren nu dat de resultaten van hun werk aan borstkanker drievoudig negatief zijn, zo genoemd omdat de tumorcellen negatief waren voor drie soorten eiwitten die bij de diagnose werden gebruikt.
Het laatste onderzoek van Lunt, gedeeltelijk gefinancierd door een nieuwe subsidie van $ 2 miljoen van de National Institutes of Health, is gepubliceerd in het tijdschrift Nature op 18 mei.
In de Nature-paper maakt Spartan deel uit van een internationaal team dat aantoont dat kankercellen met lage niveaus van het enzym fosfoglyceraatdehydrogenase, of PHGDH, een groter risico op verspreiding vormen.
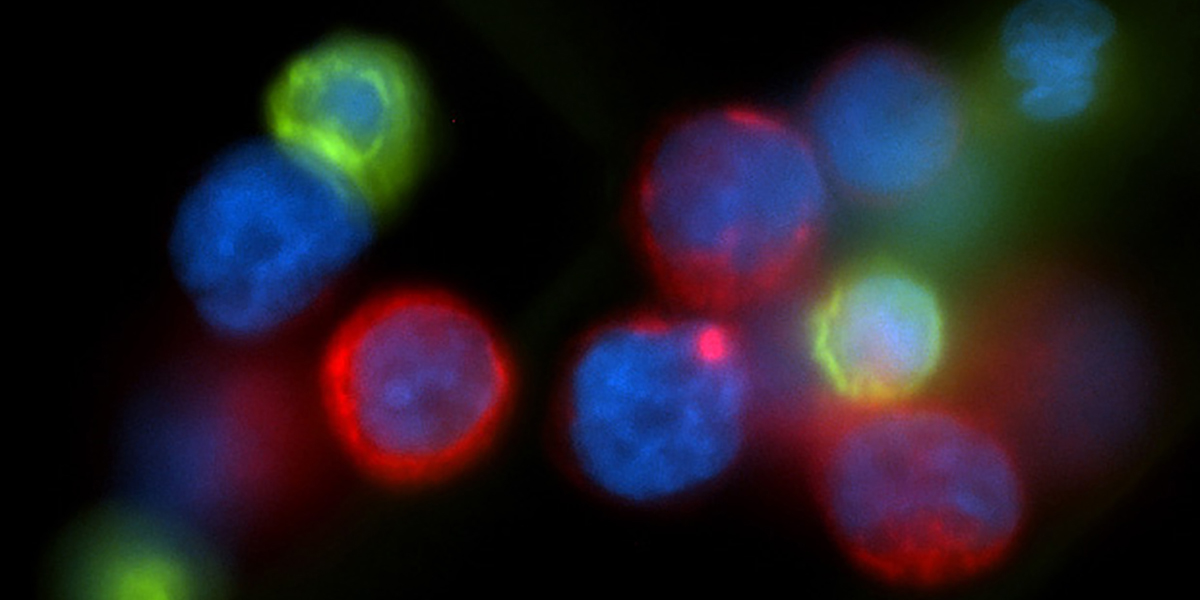
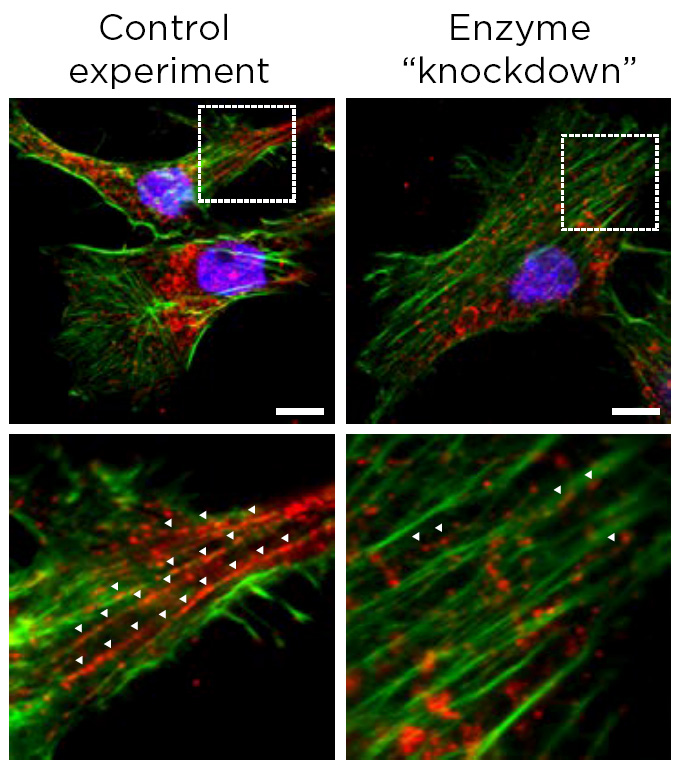
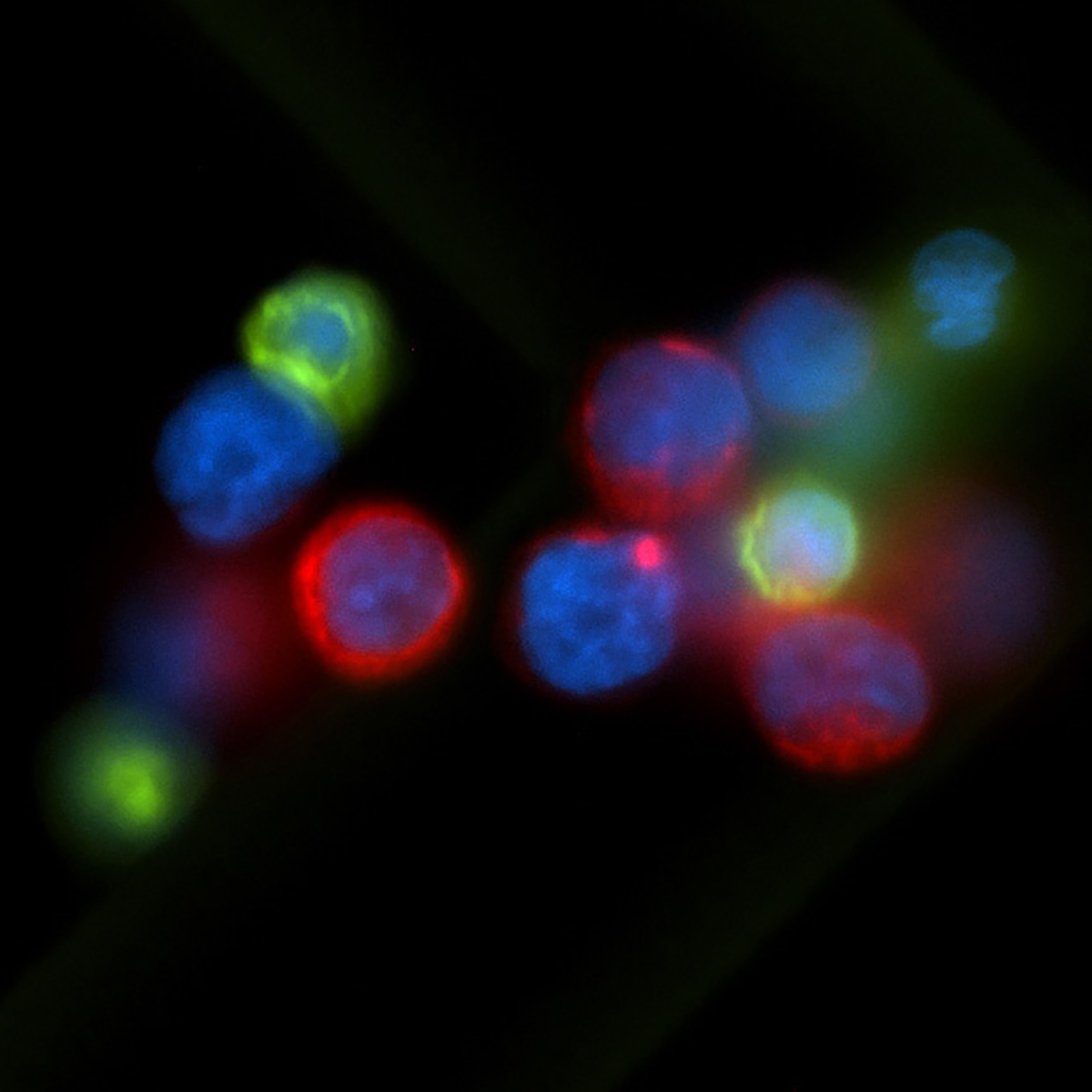
Fluorescerende microfoto’s van dit experiment helpen illustreren hoe een trapsgewijze effect kankercellen kan doen uitzaaien. Aan de linkerkant een controlemonster van een muizenkankercellijn (celkernen weergegeven in blauw) die hoge niveaus van het PHGDH-enzym tot expressie brengen, weergegeven in groen, evenals verschillende enzymen die een interactie aangaan met PHGDH, weergegeven in rood. Aan de rechterkant hebben de onderzoekers de niveaus van PHGDH verlaagd of verlaagd, wat op zijn beurt het in rood weergegeven enzym verlaagde. De afbeelding in de onderste rij toont een vergrote weergave van het rastergebied in de bovenste rij om het resultaat te vergroten. Krediet: Rossi et al., Nature
De resultaten waren aanvankelijk verrassend, zei Lunt, omdat kankercellen dit enzym ook gebruiken om zich te vermenigvuldigen. Hoe meer enzymen een tumor heeft, hoe groter de kans dat hij groeit. Lagere niveaus helpen de tumor zich echter te verspreiden. Deze bevindingen worden ondersteund door gegevens van menselijke borstkankerpatiënten en door aanvullende onderzoeken in kankercel- en muismodellen.
“We verwachtten aanvankelijk dat een hoge PHGDH-expressie de proliferatie en metastase zou ondersteunen”, zei Lunt, wiens laboratorium in Afdeling Biochemie en Moleculaire Biologie.
“De resultaten zijn echter logisch omdat de behoeften van kankercellen tijdens proliferatie en metastase heel anders zijn,” zei hij. “Tijdens proliferatie willen kankercellen zich zo snel mogelijk delen in een vertrouwde omgeving. Tijdens metastase moeten kankercellen het zeer stressvolle proces overleven van het verlaten van de primaire locatie, reizen door de bloedbaan, het vinden van nieuwe locaties en overleven in een onbekende omgeving.”
Wanneer tumoren de overvloed aan het PHGDH-enzym verminderen, kunnen andere enzymen en de processen die ze reguleren naar voren treden. In het geval van triple-negatieve borstkanker is een resultaat de productie van siaalzuur. Zuur helpt kankercellen zich tijdens metastase aan andere cellen en biologische weefselcomponenten te hechten.
Het onderzoeken van de moleculaire mechanismen die ten grondslag liggen aan deze keten van reacties en interacties is het doel van Lunts nieuwe subsidie van $ 2 miljoen, die in maart werd aangekondigd door Nationaal Kanker Instituut.
Het ontrafelen van de complexe en verwarde biochemie van kanker is een uitdaging, maar Lunt laat zien hoe het samenvoegen en uitbreiden van een wereldwijd netwerk van experts barrières op dit gebied kan helpen overwinnen.
Een microfoto die kankercellen (rood) laat zien die circuleren in het bloed van een borstkankerpatiënt. Krediet: National Cancer Institute/Norris USC Comprehensive Cancer Center/Min Yu
“Biologie is erg ingewikkeld met talloze variabelen en spelers,” zei Lunt. Om dat aan te pakken, “zijn teamwerk, samenwerking en financiering essentieel”, zei hij.
Lunt ontmoette medewerker Sarah-Maria Fendt, een kankeronderzoeker in België, voor het eerst toen ze beiden postdoctoraal onderzoekers waren aan het Massachusetts Institute of Technology.
Maar het was pas toen Fendt Lunt in 2019 een seminar over siaalzuurbiosynthese zag geven op een internationale conferentie in Florence, Italië, dat de twee met een onderzoek kwamen om samen te werken. Bij de samenwerking waren uiteindelijk onderzoekers van meer dan 30 afdelingen op drie continenten betrokken.
“Ik denk dat dergelijke grote samenwerkingen steeds gebruikelijker worden omdat we datasets van meerdere niveaus integreren en gespecialiseerde technieken gebruiken”, zegt Lunt.
De samenwerking omvat Shao Thing Teoh, die een postdoctoraal onderzoeker was in de Lunt-groep en nu een projectwetenschapper in Oostenrijk. Toen ze in 2016 bij het laboratorium van Lunt kwam, hielp ze een team met het onderzoeken van het metabolisme bij uitgezaaide borstkanker. Nu zullen Lunt en de volgende generatie van zijn cohortonderzoekers dat werk voortzetten met hun nieuwe subsidie.
Het Spartan-project onthult een nieuw molecuul dat artsen in de toekomst zouden kunnen beoordelen om de risico’s van tumoren te bepalen. Het onderzoek creëert ook een platform voor medicijnontwikkelaars om te exploiteren terwijl ze nieuwe manieren ontwikkelen om kanker aan te vallen.
“Onze studie zou kunnen leiden tot nieuwe biomarkers – zoals lage PHGDH en hoog siaalzuur – die het metastatische risico en nieuwe therapeutische doelen voor patiënten met gemetastaseerde TNBC definiëren,” zei Lunt.

“Typische tv-ninja. Popcultuurliefhebber. Webexpert. Alcoholfan. Wannabe-analist. Algemene baconliefhebber.”